表达嵌合抗原受体(CAR)的基因工程T细胞正在迅速发展,有望用于血液学和非血液学恶性肿瘤的治疗。CAR-T疗法可引起快速而持久的临床反应,但常出现急性毒性等副作用。近期,Nature子刊杂志发表了海军军医大学基础医学部的研究论文。研究人员发现CAR-T细胞会释放表面表达CAR的外泌体,含CAR的外泌体能显著抑制肿瘤生长并且安全性较好,是一种潜在的新的抗肿瘤治疗方法。
基于嵌合抗原受体(CARs)或T细胞受体(TCRs)的基因工程自体细胞、或同种异体T细胞作为细胞免疫疗法的应用正在成为一种有前景的新治疗方法。众多I / II期临床试验数据表明,对于标准疗法难治的B细胞恶性肿瘤,这种方法通常可使总体缓解率达到50-90%。但过继性T细胞疗法往往产生出明显毒性,最常见的两种毒性作用是细胞因子释放综合征(cytokine release syndrome,CRS),其特征是高烧、低血压、缺氧或多器官毒性;以及CAR-T相关性脑病综合征 (CAR-T-related encephalopathy syndrome,CRES,通常以毒性脑病状态为特征,其表现为妄想症、神志不清,偶尔还有脑水肿和癫痫发作。尽管在治疗难治性血液系统恶性肿瘤患者中观察到CAR-T细胞有强烈应答,但在实体瘤中的结果却比较有限。这可能是由于实体肿瘤的肿瘤微环境(TME)中存在着许多障碍,比如由上调抑制性受体(IR)介导的内在抑制途径引起治疗不佳,这些抑制受体对CAR-T细胞在肿瘤中的同源配体例如PD1信号等会发生反应。
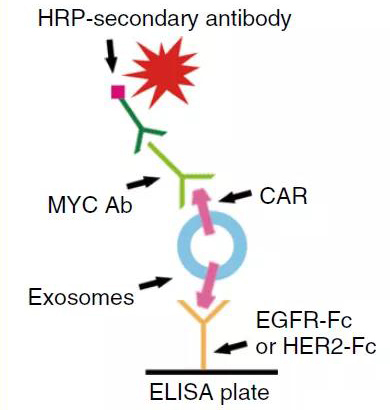
基于外泌体的生物学特性,源自CAR-T细胞的外泌体在免疫治疗中具有直接攻击的作用。因为外泌体与类似于脂质体的合成药物载体具有功能和结构上的相似性,所以外泌体可以进一步用于药物递送。但是,由于CAR-T细胞的靶向特异性是由CAR结构中抗体衍生的scFv决定的,因此直接从CAR-T细胞培养基中分离的外泌体可能具有异质性,并且可能失去靶向特异性。这些数据表明,源自CAR-T细胞的纯化含CAR外泌体可用作癌症靶向剂,并可以改善现有的治疗效果。
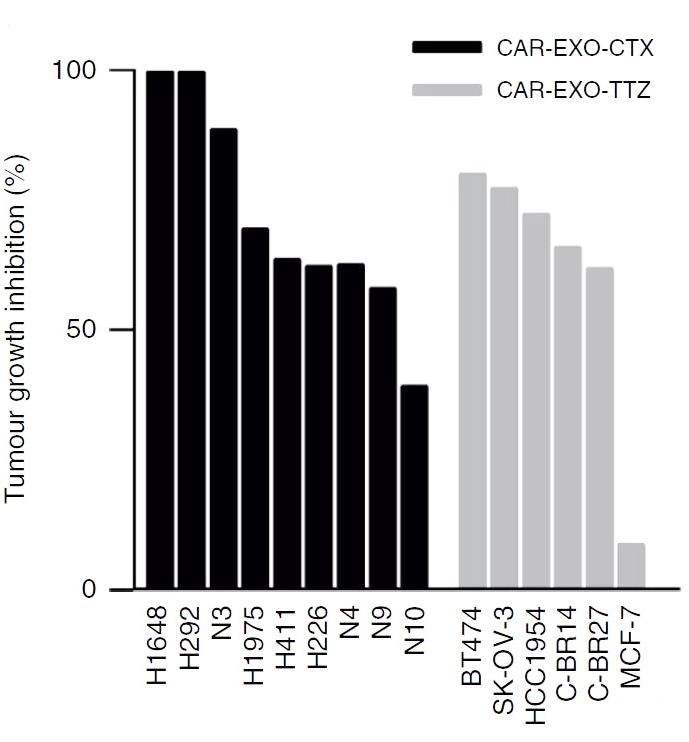
原文报道:CAR exosomes derived from effector CAR-T cells have potent antitumour effects and low toxicity.
Nat Commun. 2019 Sep 25;10(1):4355.
论文作者:Fu W, Lei C, Liu S, Cui Y, Wang C, Qian K, et al.
上海舜纳生物科技有限公司 纳米医学技术研发中心 Sunlipo Biotech Research Center for Nanomedicine
邮箱:sunlipotech@163.com(技术服务)info@med-nanotech.com(应用开发)
电话:86-21-5127 9909 传真:86-21-5193 6393
-
2020-11-25
-
2020-01-12
-
2019-12-10
-
2017-06-01
-
2017-04-21
-
2017-04-09
-
2017-01-17
-
2017-01-17
- ▪ 2020国自然生物医工项目(重点、面上项目)
- ▪ 2020国自然生物医工项目(地区、青年项目)
- ▪ 2019国自然生物医工项目(重点、面上项目)
- ▪ 2019国自然生物医工项目(地区、青年项目)
- ▪ 舜纳医工新型全氟丙烷微泡超声造影剂(研发级)发布上市
- ▪ 科研用巨噬细胞清除剂(氯磷酸二钠脂质体Clodronate Liposomes)量产上市
- ▪ 舜纳纳米受邀在“创新绍兴”成果对接会进行《医工交叉研究技术服务和新型纳米医药研发平台》主题交流
- ▪ 小核酸药物引领生物医药变革(核酸药物载体技术)
- ▪ 可注射仿生水凝胶高效修复半月板、软骨等骨关节损伤技术
- ▪ 舜纳纳米功能胶束载药技术——助力上海市重点项目转化应用
- ▪ 新型抗肿瘤生物治疗药物——抗肿瘤核酸疫苗 (舜纳纳米 免疫载体)
- ▪ 肿瘤疫苗增效新思路:皮下注射智能水凝胶技术
- ▪ CAR-T细胞分泌的外泌体具有高效低毒抗肿瘤作用
- ▪ 新型紫杉醇胶束Apealea(paclitaxel micellar)获欧盟批准上市
- ▪ 2018国自然生物医工项目(重大及面上项目)汇总分析