当前位置:首页 >
PH敏感脂质体的设计概述 (舜纳纳米 智能响应载体)
来源于:纳米医学网 | 作者:小N | 发布时间:2017-02-15 | 浏览:6849
脂质体是具有双层膜的封闭式粒子。脂质体技术主要是利用生物膜的物理化学性质作为药物载体。脂质体转运DNA原理是脂质体加速大分子、荷电多的分子透过细胞膜。此过程相当复杂,尤其在包封较大片段上。由于这种技术在实践中只在体外使用且要用融合剂,荷电越多用途越少;同时由于脂质体稳定性和在环境中相互作用的特点而不能广泛使用。采用pH敏脂质体可以改善转运并且不改变方向。立体稳定性的pH-敏脂质体在血循环中极稳定,避免了在血循环中被迅速清除,可在血管部位渗出并在肿瘤组织发挥作用,已成功地用于人体肿瘤治疗的临床前和临床试验。
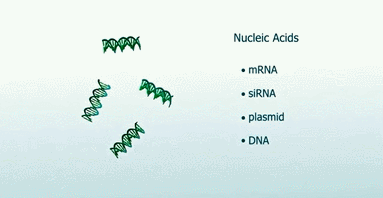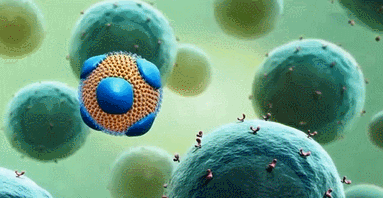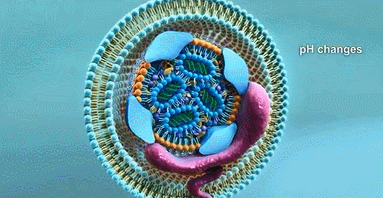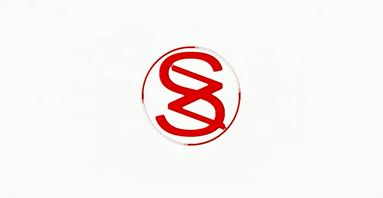
pH-敏脂质体是一种具有细胞内靶向和控制药物(如基因、核酸、肽、蛋白质)释放的功能性脂质体。其原理是pH低时可导致脂肪酯羧基的质子化而引起六角晶相的形成,这是膜融合的主要机制。在酸性条件下,即在核内体(endosome)形成后几分钟内,进入溶酶体之前, pH从7.4减至5.3~6.3左右时,pH-敏脂质体膜发生结构改变,促使脂质体膜与核内体/溶酶体膜的融合,将包封的物质导入胞浆及主动靶向病变组织,避免网状内皮系统的清除。制成pH敏脂质体可在一定程度上避免溶酶体降解并增加包封物摄取量和稳定性,有效地将包封物转运到胞浆。
1 pH-敏脂质体设计
pH-敏脂质体的组成影响pH-敏脂质体的pH敏感性。由于脂膜中含有不饱和PE(磷脂酰胺),不易水化,它在中性生理环境下可形成六角晶相,须加入某些脂肪酸以制成稳定的脂质。当pH<6.5时,脂肪酸的羟基端质子化,形成六角晶相引起膜的融合,这一点已用共振能量转换分析(resonance energy transfer assay)证实。脑硫脂对二硫酰磷脂酰胺(DOPE)小单室脂质体有双重稳定作用,脑硫脂是一种酸性糖脂,含有疏水基和一种可水化及硫化的残基。摩尔百分比为30的脑硫脂和摩尔百分比为50的DOPE在N2保护下超声后转移到试管中,用N2挥干;样品在真空条件4℃贮存24 h。试管壁上的脂薄膜用缓冲液水化,在N2保护、冰浴下超声10 min,即得。
两亲极性组成的pH敏脂质体,作为一种可质子化的成分9 组成为可离子化的跨膜两亲极性物质——二半琥珀酰氧己基-粘康酸酯(DHM)的脂质体,其在各种pH的磷酸盐缓冲液中, 37℃孵育1 h显示出pH敏的特点。 即在中性pH时脂质体是稳定的, 在酸性条件下是不稳定的。组成为DOPE和二硫酰磷脂酰胆碱(DOPC)(摩尔比1∶1)脂质体在弱酸条件下无不稳定性,表明DHM作为脂质体的一个酸性成分。由于DHM中粘性基团为硬性部分,能防止两亲物质在脂质体膜中变为U型,同时防止酸性成分受外界血清的影响,所以DHM组成的pH敏脂质体在37℃血浆中稳定。
pH-敏脂质体在心血管疾病基因治疗中也得到应用。利用病毒细胞融合脂质体的特点,将日本血细胞凝集病毒(HVJ)与脱氧寡核苷酸或质粒DNA脂质体复合,能诱导DNA直接进入细胞浆。另外,DNA连接的核蛋白经HVJ-脂质体包封增强了质粒基因表达,表明:融合病毒基因脂质体能有效地在体内、外介导寡聚脱氧核苷酸和基因片段;同时表明,这种脂质体适宜在多种动物组织的靶向DNA转移。目前已成功地应用这种基因治疗手段治疗心血管增生,例如用反义脱氧寡核苷酸融合基因病毒脂质体对抗细胞循环基因等。
2 pH-敏免疫脂质体设计
pH敏免疫脂质体是靶向细胞的有效载体。作用机制为受体介导的内吞作用。脂质体进入核内体或溶酶体的酸性环境中不稳定并且变成融合成分,表明该新型脂质体是一种有效的质粒DNA转运系统(抗癌药)。病毒茶叶碱激酶基因的质粒包入表面嵌合抗体的靶向脂质体,这些脂质体显示出长期DNA活性,且对靶细胞有效。机制为pH-敏脂质体诱导核内体或溶酶体部分溶解,表明有效的胞浆转运。pH-敏脂质体是相对大量的稳定制剂,转染可采用将脂质体与质粒DNA混合的方法导入细胞。
流感病毒通过内吞途径而感染细胞,细胞内的空泡内为弱酸性(pH 5~6),酸性pH触发了血液凝集素蛋白的改变,并促进病毒膜与核内体融合。由这一机制设计的在中性pH时脂双层结构,在酸性pH时通过膜-膜融合而发生胶团转变的pH敏免疫脂质体6,显示体内基因靶向的特点,经结合单克隆抗体的pH敏脂质体,显著提高对肿瘤细胞表面抗原的靶向性。将脂质体结合肿瘤细胞表面抗原的抗体经小鼠腹膜内给药,进而表达质粒编码的在诱导启动子后的报告基因。表明:在给抗体靶向的pH敏脂质体肿瘤细胞内的报告基因活性最高。
pH-敏免疫脂质体在大鼠神经元(neuron)和神经蚀质(glial)的转染实验表明:抗体5-113(导向大鼠神经蚀质细胞外表面抗原)、抗体THy1.1和一种非免疫抗体通过N-戊二酰基-磷脂酰胺结合型脂质体,包封标记的质粒后,可在神经原、星型细胞、血细胞中见到X-gal反应产物。动物注射抗体THy1.1结合脂质体后,在神经原处标记物的量增加,同时动物注射抗体5-113结合脂质体后,在神经蚀质处的标记物量增加。在脊髓中,免疫脂质体穿透距离较大,从注射部位经几厘米转染神经原。这些资料表明:该脂质体包封β-半乳糖苷酶(β-galactosidase)质粒可控制细胞巨化病毒启动子。采用3种不同抗体之一构建的脂质体注入成年大鼠脑或脊髓腔内,在神经系统基因转运上免疫脂质体为有效转染系统。
pH敏免疫脂质体能提高寡核苷酸在人骨髓和淋巴白细胞内的转运,实验表明:细胞摄取脂质体包封的抗-myb寡核苷酸比摄取游离型寡核苷酸量高3~5倍。另外,带有专一性抗体如抗-CD32或抗-CD2的免疫脂质体与白血病细胞上受体的作用使寡核苷酸转运至白血病细胞效果增强, 其摄取量为单独采用脂质体或非专属性脂质体使人白血病细胞摄取量的2倍。免疫脂质体经过特定的抗体连接促进寡核苷酸进入有合适受体的白血病细胞。
结合棕榈酰抗体的磷脂酰胺pH-敏脂质体主动靶向细胞,提高包封的阿糖胞苷或无环鸟苷的抗病毒效果和细胞毒性。小鼠感染单疱疹病毒的纤维细胞L929在低的分裂期时应用阿糖胞苷靶敏感性免疫脂质体(组成为磷脂酰胺)能有效地抑制病毒复制并且细胞毒性比游离药物低。细胞毒性结果表明:游离的阿糖胞苷、pH敏感阿糖胞苷脂质体CD50分别为0.3 ng/ml和1 μg/ml,包封的阿糖胞苷病毒抑制半数有效量ED50为1.8 ng/ml,而同等的抗病毒活性则要求游离药物浓度剂量至少高1 000倍,表明pH敏免疫脂质体在药物转运上的优越性,特别是对有细胞性的药物转运更有效。采用靶非敏感免疫脂质体可在某些程度上使活性增强,但比靶敏感免疫脂质体低7倍;该结果也说明经靶敏感免疫脂质体的细胞核苷转运系统为专一性位点的核苷类似物转运的作用机制。
3 长内循pH-敏脂质体设计
细胞内立体稳定的pH-敏脂质体转运水溶性物质并延长体内循环时间。在弱酸性pH条件下,不稳定的脂质体为转运水溶性药物进入胞浆的有效载体。然而,体内使用则因被网状内皮系统摄取而受限制。由于聚乙二醇-磷脂酰胺(PEG-PE)有立体稳定作用而延长脂质体的循环时间。这一修饰显著降低了脂质体内pH依赖性的荧光标记降钙素的释放,而且降钙素从脂质体中释放后被细胞内化,同时受到核内体酸化作用的抑制剂氯化铵的限制,显示其体内独特性质。大鼠静脉注射二油酰磷脂酰胺/PEG-PE脂质体后,碘的分布动力学的药动学参数与立体稳定的二硬脂酰磷脂酰胆碱/PEG-PE脂质体相似。反之,无PEG-PE成分的pH-敏脂质体则被迅速清除,立体稳定的pH-敏脂质体对体内转运基因、反义核苷酸和核酶等高密度阴离子分子很有潜力。
4 聚合物修饰的pH-敏脂质体设计
pH-敏聚乙二醇衍生物修饰的蛋黄卵磷脂脂质体介导降钙素的细胞浆给药组成为磷脂酰胆碱和聚乙二醇衍生物(琥珀酰化聚缩水甘油)的一种新型脂质体,在弱酸或酸性条件下具有融合能力。降钙素由琥珀酰化聚缩水甘油修饰的脂质体向胞浆转运。CV-1细胞、绿猴肾细胞与非修饰降钙素脂质体在37℃孵育,胞浆内降钙素发散微弱的荧光,相反,聚合物修饰的降钙素脂质体则显示出很强的发散荧光,表明降钙素转运至细胞浆。表明:用大量的聚合物修饰脂质体使胞浆转染更有效。融合分析显示,在修饰脂质体和核内体和/或溶酶体膜之间,发生了融合。而且,用大量聚合物修饰脂质体在细胞内化后具有更高的融合百分率。在细胞内吞后,共振能量转换分析显示在聚合物修饰的脂质体和核内体/或溶酶体膜之间发生了融合。并且,聚合物含量越高内吞后融合百分率越高。这些结果表明,通过细胞内吞途径,在细胞内化后经过与核内体膜融合,聚合物修饰脂质体转运内含物进入胞浆。
总之,pH-敏脂质体的研究,越来越离不开对细胞内细胞器的相互作用、融合、释放及体内过程的探索,从而有针对性地载药、释药,最终达到靶向目的;药剂学上pH-敏脂质体技术水平的提高也越来越离不开与生化、生理、药理、分子生物学等学科的联系与融合。具体可关注我们所供应纳米产品等——核酸抗肿瘤疫苗载体(iV, iP, iH免疫因子载体)。
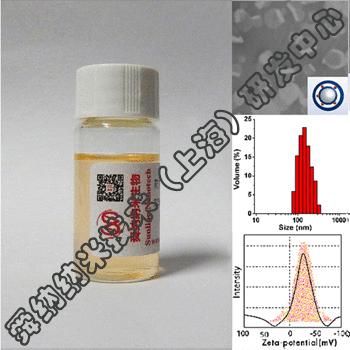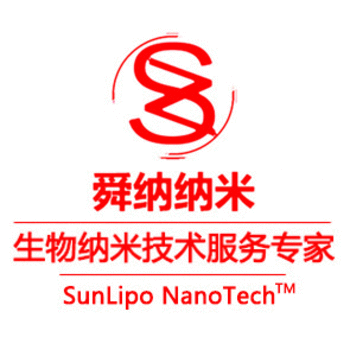

值得分享的是,舜纳纳米自成立以来,坚持“专注转化 服务医工”的践行理念,先后为多家上市生物医药及创新器械企业提供生物纳米技术开发,并与全国近百家医疗单位开展纳米医疗技术研发合作,有效开展医工交叉实践,获得了良好的产业信任与业内口碑;并依托纳米医学网将自身的优势技术与医疗平台的“辐射”能力,加速推进新材料、新技术在免疫、肿瘤、心血管、骨科、眼科、皮肤等六大临床中心的实践转化,积极促进合作技术项目的开发及转化。在可见的未来,舜纳将与医工各界人士深入合作,为健康医疗事业提供更好的服务与产品。
上海舜纳生物科技有限公司 纳米医学技术研发中心 Sunlipo Biotech Research Center for Nanomedicine
邮箱:sunlipotech@163.com(技术服务)info@med-nanotech.com(应用开发)
电话:86-21-5127 9909 传真:86-21-5193 6393
阳离子纳米复合、siRNA脂质体、阳离子聚合物、pamam、核酸PAMAM、阳离子高分子、树枝物、相关研发应用
-
2021-01-31
-
2021-01-05
-
2020-11-25
-
2020-11-25
-
2020-05-21
-
2020-01-22
-
2019-01-27
-
2017-12-31
疾病应用(检索)
热门文章
- ▪ 2020国自然生物医工项目(重点、面上项目)
- ▪ 2020国自然生物医工项目(地区、青年项目)
- ▪ 2019国自然生物医工项目(重点、面上项目)
- ▪ 2019国自然生物医工项目(地区、青年项目)
- ▪ 舜纳医工新型全氟丙烷微泡超声造影剂(研发级)发布上市
- ▪ 科研用巨噬细胞清除剂(氯磷酸二钠脂质体Clodronate Liposomes)量产上市
- ▪ 舜纳纳米受邀在“创新绍兴”成果对接会进行《医工交叉研究技术服务和新型纳米医药研发平台》主题交流
- ▪ 小核酸药物引领生物医药变革(核酸药物载体技术)
- ▪ 可注射仿生水凝胶高效修复半月板、软骨等骨关节损伤技术
- ▪ 舜纳纳米功能胶束载药技术——助力上海市重点项目转化应用
- ▪ 新型抗肿瘤生物治疗药物——抗肿瘤核酸疫苗 (舜纳纳米 免疫载体)
- ▪ 肿瘤疫苗增效新思路:皮下注射智能水凝胶技术
- ▪ CAR-T细胞分泌的外泌体具有高效低毒抗肿瘤作用
- ▪ 新型紫杉醇胶束Apealea(paclitaxel micellar)获欧盟批准上市
- ▪ 2018国自然生物医工项目(重大及面上项目)汇总分析




